Etika dan Potensi CRISPR dalam Menyembuhkan Penyakit Genetik: Menjelajahi Batasan Ilmiah dan Moral
Di era modern ini, kemajuan ilmu pengetahuan dan teknologi telah membuka pintu menuju solusi-solusi inovatif untuk tantangan kesehatan yang paling mendesak. Salah satu terobosan paling revolusioner dalam bioteknologi adalah teknologi pengeditan gen CRISPR-Cas9 (Clustered Regularly Interspaced Short Palindromic Repeats). Teknologi ini menjanjikan harapan besar untuk menyembuhkan berbagai penyakit genetik yang sebelumnya dianggap tidak dapat diobati.
Namun, kekuatan transformatif CRISPR juga membawa serta serangkaian pertanyaan etis yang kompleks dan mendalam. Artikel ini akan mengulas secara komprehensif etika dan potensi CRISPR dalam menyembuhkan penyakit genetik, menyoroti janji-janji ilmiahnya, serta dilema moral dan sosial yang harus kita hadapi sebagai masyarakat global.
Apa Itu CRISPR-Cas9? Gunting Molekuler untuk Genom Manusia
Sebelum kita menyelami lebih jauh potensi dan etika, penting untuk memahami apa itu CRISPR-Cas9. Singkatnya, CRISPR adalah teknologi revolusioner yang memungkinkan para ilmuwan untuk mengedit bagian-bagian tertentu dari DNA dengan presisi yang belum pernah terjadi sebelumnya. Ia sering diibaratkan sebagai "gunting molekuler" yang sangat canggih.
Mekanisme Kerja yang Revolusioner
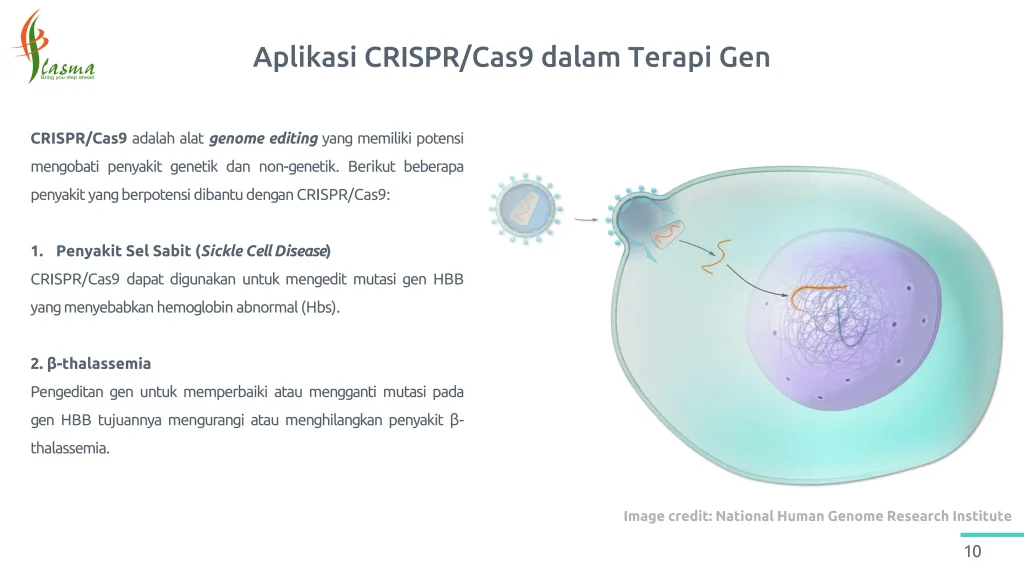
Sistem CRISPR-Cas9 berasal dari sistem pertahanan alami bakteri terhadap virus. Ia bekerja dengan menggunakan molekul panduan RNA (gRNA) untuk mengarahkan enzim Cas9 ke lokasi spesifik pada untai DNA. Setelah target ditemukan, enzim Cas9 akan memotong DNA pada lokasi tersebut, memungkinkan para ilmuwan untuk menghilangkan, menambahkan, atau mengganti segmen DNA yang rusak atau tidak diinginkan. Proses ini dapat memperbaiki mutasi genetik penyebab penyakit atau bahkan menonaktifkan gen yang merugikan.
Sejarah Singkat Penemuan dan Perkembangan
Konsep CRISPR pertama kali ditemukan pada bakteri pada akhir 1980-an, tetapi potensinya sebagai alat pengeditan gen baru disadari dan dikembangkan pada awal 2010-an. Para peneliti seperti Jennifer Doudna dan Emmanuelle Charpentier memainkan peran kunci dalam adaptasi teknologi ini untuk digunakan pada sel eukariotik, termasuk sel manusia, yang mengantarkan mereka pada Hadiah Nobel Kimia pada tahun 2020. Penemuan ini telah mengubah lanskap biologi molekuler dan terapi genetik secara fundamental.
Potensi CRISPR dalam Menyembuhkan Penyakit Genetik
Etika dan potensi CRISPR dalam menyembuhkan penyakit genetik adalah dua sisi mata uang yang tidak terpisahkan. Potensi terapeutik CRISPR sangatlah luas, menawarkan harapan baru bagi jutaan orang yang menderita kondisi genetik.
Penyakit Monogenik: Target Utama yang Menjanjikan
Penyakit monogenik adalah kondisi yang disebabkan oleh mutasi pada satu gen tunggal. Ini adalah target paling menjanjikan untuk terapi CRISPR karena permasalahannya relatif terdefinisi dengan baik.
- Anemia Sel Sabit (Sickle Cell Disease): Penyakit darah ini disebabkan oleh mutasi pada gen hemoglobin. CRISPR dapat digunakan untuk mengoreksi mutasi ini pada sel punca hematopoietik pasien, berpotensi menyembuhkan penyakit.
- Beta-Talasemia: Mirip dengan anemia sel sabit, talasemia juga merupakan kelainan darah genetik. Uji klinis awal menggunakan CRISPR menunjukkan hasil yang menjanjikan dalam mengoreksi gen yang rusak dan mengurangi kebutuhan transfusi darah.
- Fibrosis Kistik (Cystic Fibrosis): Penyakit ini memengaruhi paru-paru dan sistem pencernaan akibat mutasi pada gen CFTR. CRISPR sedang dieksplorasi untuk memperbaiki gen ini, meskipun tantangan dalam pengiriman ke sel target masih signifikan.
- Penyakit Huntington: Sebuah penyakit neurodegeneratif progresif yang disebabkan oleh gen yang bermutasi. CRISPR dapat digunakan untuk menonaktifkan gen penyebab penyakit atau mengoreksi mutasinya.
Menjelajahi Penyakit Kompleks: Tantangan dan Harapan Masa Depan
Selain penyakit monogenik, CRISPR juga memiliki potensi untuk mengatasi penyakit kompleks yang melibatkan banyak gen atau interaksi gen-lingkungan.
- Kanker: CRISPR dapat digunakan untuk memodifikasi sel T (jenis sel imun) pasien agar lebih efektif dalam mengenali dan menyerang sel kanker. Ini adalah dasar dari imunoterapi yang dimediasi sel CAR-T yang sedang berkembang pesat.
- Penyakit Jantung: Beberapa bentuk penyakit jantung memiliki komponen genetik yang kuat. CRISPR dapat menargetkan gen-gen yang terlibat dalam pembentukan plak aterosklerotik atau kondisi jantung bawaan.
- Infeksi Virus: CRISPR juga menunjukkan potensi dalam memerangi infeksi virus persisten seperti HIV atau Herpes Simplex Virus, dengan memotong DNA virus dari genom sel inang.
Pendekatan Ex Vivo dan In Vivo dalam Terapi CRISPR
Penerapan CRISPR dalam terapi genetik dapat dilakukan melalui dua pendekatan utama:
- Pendekatan Ex Vivo: Sel-sel pasien (misalnya, sel punca darah) diambil dari tubuh, diedit di laboratorium menggunakan CRISPR, kemudian dikembalikan ke tubuh pasien. Pendekatan ini lebih mudah dikontrol dan memiliki risiko efek samping yang lebih rendah.
- Pendekatan In Vivo: Sistem CRISPR langsung dikirim ke dalam tubuh pasien untuk mengedit sel-sel di lokasi yang diinginkan (misalnya, hati, mata, atau otak). Pendekatan ini lebih menantang dalam hal pengiriman yang aman dan efisien, serta kontrol terhadap efek samping.
Aplikasi Luas di Luar Terapi Langsung
Selain terapi langsung, CRISPR juga menjadi alat yang tak ternilai dalam penelitian biomedis, memungkinkan para ilmuwan untuk:
- Memodelkan Penyakit: Menciptakan model penyakit genetik pada hewan atau sel untuk memahami mekanisme penyakit dan menguji terapi baru.
- Penemuan Obat: Mengidentifikasi gen-gen yang terlibat dalam jalur penyakit dan mencari target obat baru.
- Diagnostik Cepat: Mengembangkan alat diagnostik yang cepat dan akurat untuk mendeteksi patogen atau mutasi genetik.
Perkembangan Uji Klinis dan Kasus Sukses Awal
Potensi transformatif CRISPR bukan lagi sekadar teori. Berbagai uji klinis telah dimulai di seluruh dunia, menunjukkan hasil yang menjanjikan. Sebagai contoh, pasien dengan anemia sel sabit dan beta-talasemia yang menjalani terapi CRISPR ex vivo telah menunjukkan peningkatan signifikan, bahkan remisi penyakit pada beberapa kasus. Demikian pula, uji klinis untuk penyakit mata genetik seperti Leber Congenital Amaurosis menggunakan pendekatan in vivo telah menunjukkan perbaikan penglihatan pada beberapa pasien.
Meskipun hasil awal ini sangat menggembirakan, penting untuk diingat bahwa sebagian besar terapi ini masih dalam tahap eksperimental. Penelitian lebih lanjut dan pengawasan jangka panjang diperlukan untuk sepenuhnya memahami keamanan dan efektivitas jangka panjang dari terapi CRISPR.
Etika CRISPR dalam Menyembuhkan Penyakit Genetik: Batasan Moral dan Sosial
Seiring dengan janji-janji ilmiahnya yang luar biasa, etika dan potensi CRISPR dalam menyembuhkan penyakit genetik juga memunculkan serangkaian pertanyaan moral yang mendalam. Kemampuan untuk memodifikasi genom manusia secara fundamental memaksa kita untuk merenungkan batasan-batasan yang tidak boleh dilanggar.
Efek Off-Target dan Keamanan Jangka Panjang
Salah satu kekhawatiran utama adalah kemungkinan efek off-target, di mana enzim Cas9 memotong DNA di lokasi yang tidak diinginkan. Pemotongan yang salah ini dapat menyebabkan mutasi baru yang berpotensi berbahaya, termasuk risiko kanker. Meskipun teknologi CRISPR terus disempurnakan untuk meningkatkan presisi, risiko ini masih menjadi perhatian serius dan memerlukan pengawasan ketat. Keamanan jangka panjang dari sel-sel yang diedit CRISPR dalam tubuh manusia juga masih belum sepenuhnya dipahami.
Penyuntingan Sel Somatik vs. Sel Germinal: Dilema Etis yang Krusial
Ini adalah inti dari perdebatan etis seputar CRISPR.
- Penyuntingan Sel Somatik: Melibatkan pengeditan gen pada sel-sel tubuh non-reproduktif (sel somatik) seorang individu. Perubahan genetik ini hanya akan memengaruhi individu yang dirawat dan tidak akan diturunkan kepada keturunannya. Sebagian besar komunitas ilmiah dan etis umumnya menerima penyuntingan sel somatik untuk tujuan terapeutik, asalkan aman dan efektif.
- Penyuntingan Sel Germinal: Melibatkan pengeditan gen pada sel reproduktif (sperma, sel telur) atau embrio awal. Perubahan genetik ini akan diwariskan ke generasi berikutnya dan menjadi permanen dalam garis keturunan manusia. Inilah yang memicu kekhawatiran terbesar.
Kekhawatiran seputar penyuntingan sel germinal meliputi:
- "Bayi Desainer" dan Eugenika: Kekhawatiran bahwa CRISPR dapat digunakan untuk menciptakan "bayi desainer" dengan sifat-sifat yang diinginkan (misalnya, kecerdasan, penampilan fisik) daripada hanya mengoreksi penyakit. Ini dapat mengarah pada bentuk eugenika baru, di mana masyarakat mulai memilih sifat-sifat manusia dan menciptakan ketidaksetaraan genetik yang lebih dalam.
- Perubahan Permanen pada Genom Manusia: Perubahan yang dilakukan pada sel germinal tidak dapat diubah dan akan memengaruhi semua keturunan di masa depan. Konsekuensi jangka panjang dari perubahan ini terhadap evolusi manusia dan keanekaragaman genetik masih belum diketahui.
- Otonomi dan Persetujuan: Bagaimana kita bisa mendapatkan persetujuan dari individu yang belum lahir atau belum ada untuk perubahan genetik yang akan memengaruhi mereka?
Mengingat risiko dan implikasi etis yang sangat besar, sebagian besar negara dan organisasi ilmiah global telah menyerukan moratorium atau larangan ketat terhadap penyuntingan sel germinal manusia untuk saat ini.
Aksesibilitas, Keadilan, dan Komersialisasi
Jika terapi CRISPR terbukti efektif, siapa yang akan memiliki akses ke dalamnya?
- Ketidaksetaraan Kesehatan: Terapi genetik kemungkinan akan sangat mahal pada awalnya, menciptakan kesenjangan antara mereka yang mampu membayar dan mereka yang tidak. Ini dapat memperburuk ketidaksetaraan kesehatan global yang sudah ada.
- Komersialisasi yang Tidak Etis: Ada risiko komersialisasi yang tidak etis, di mana perusahaan memprioritaskan keuntungan daripada kesejahteraan pasien atau implikasi etis yang lebih luas.
- Prioritas Penyakit: Penyakit mana yang akan diprioritaskan untuk terapi CRISPR? Apakah penyakit yang langka akan mendapatkan perhatian yang sama dengan penyakit yang lebih umum?
Persetujuan Berinformasi dan Otonomi Pasien
Untuk terapi CRISPR yang disetujui, penting untuk memastikan bahwa pasien sepenuhnya memahami sifat eksperimental, risiko, dan potensi manfaat dari perawatan. Mengingat kompleksitasnya, proses persetujuan berinformasi harus sangat cermat dan transparan.
Pandangan Filosofis dan Religius
Banyak pandangan filosofis dan religius mempertanyakan etika memanipulasi genom manusia. Beberapa melihatnya sebagai "bermain Tuhan" atau melampaui batas-batas alamiah yang ditetapkan. Diskusi ini menambah lapisan kompleksitas pada perdebatan etis.
Regulasi dan Pengawasan Global
Mengingat sifat global ilmu pengetahuan dan potensi dampak lintas batas dari teknologi CRISPR, diperlukan kerangka kerja regulasi dan pengawasan internasional yang kuat. Ini akan membantu memastikan pengembangan yang bertanggung jawab, mencegah penyalahgunaan, dan mempromosikan keadilan dalam akses.
Tantangan Ilmiah dan Batasan Teknologi CRISPR
Selain dilema etis, CRISPR juga menghadapi tantangan ilmiah yang signifikan yang perlu diatasi sebelum potensinya dapat direalisasikan sepenuhnya.
- Metode Pengiriman yang Efisien dan Aman: Salah satu hambatan terbesar adalah bagaimana mengirimkan komponen CRISPR (gRNA dan Cas9) secara efisien dan aman ke sel-sel target yang tepat di dalam tubuh, terutama untuk organ yang sulit dijangkau seperti otak atau paru-paru.
- Respons Imun: Tubuh mungkin mengenali komponen CRISPR (terutama protein Cas9) sebagai benda asing dan memicu respons imun, yang dapat menetralkan terapi atau menyebabkan efek samping.
- Efisiensi Pengeditan dan Mozaikisme: Tidak semua sel dalam jaringan target akan berhasil diedit, yang dapat menyebabkan kondisi yang disebut mozaikisme. Efisiensi pengeditan yang rendah dapat mengurangi efektivitas terapi.
- Biaya Tinggi: Pengembangan dan penerapan terapi CRISPR saat ini sangat mahal, menjadikannya tidak terjangkau bagi sebagian besar populasi dunia.
Masa Depan CRISPR: Inovasi dan Diskusi Berkelanjutan
Meskipun tantangan dan pertanyaan etis masih ada, teknologi CRISPR terus berkembang pesat.
Teknologi Pengeditan Gen Generasi Baru
Peneliti terus mengembangkan varian CRISPR yang lebih canggih, seperti base editing dan prime editing. Teknologi ini menawarkan presisi yang lebih tinggi, kemampuan untuk membuat perubahan yang lebih halus pada DNA, dan potensi untuk mengurangi efek off-target. Inovasi ini dapat mengatasi beberapa kekhawatiran keamanan yang ada saat ini.
Kebutuhan akan Dialog Etis dan Transparansi
Masa depan CRISPR akan sangat bergantung pada dialog etis yang berkelanjutan dan transparan antara ilmuwan, pembuat kebijakan, etikus, pasien, dan masyarakat luas. Penting untuk membangun konsensus tentang batasan yang dapat diterima dan cara terbaik untuk memanfaatkan teknologi ini demi kebaikan umat manusia. Pendidikan publik tentang CRISPR juga krusial untuk memastikan keputusan dibuat secara informatif.
Kolaborasi Global
Kolaborasi internasional akan menjadi kunci untuk menetapkan standar etika dan regulasi yang konsisten, berbagi pengetahuan, dan memastikan bahwa manfaat CRISPR dapat diakses secara adil di seluruh dunia.
Kesimpulan
Etika dan potensi CRISPR dalam menyembuhkan penyakit genetik merepresentasikan salah satu babak paling menarik dan menantang dalam sejarah kedokteran. Teknologi ini menawarkan harapan luar biasa untuk mengakhiri penderitaan akibat penyakit genetik yang tak tersembuhkan, dengan potensi untuk mengubah kehidupan jutaan orang. Namun, kekuatan yang luar biasa ini juga menuntut tanggung jawab yang tidak kalah besar.
Kita berdiri di persimpangan jalan di mana inovasi ilmiah bertemu dengan pertanyaan-pertanyaan mendasar tentang apa artinya menjadi manusia. Untuk memaksimalkan manfaat CRISPR dan meminimalkan risikonya, kita harus mengadopsi pendekatan yang hati-hati, memprioritaskan keamanan pasien, memastikan keadilan akses, dan terlibat dalam diskusi etis yang terbuka dan berkelanjutan. Dengan regulasi yang kuat, pengawasan yang cermat, dan komitmen terhadap nilai-nilai kemanusiaan, CRISPR dapat menjadi kekuatan transformatif untuk kebaikan yang akan mendefinisikan kembali masa depan pengobatan genetik.